A血型救治、o型血可以救a型血吗
- 作者:
- 来源: 水镜先生网
- 2025-04-15 00:38:02
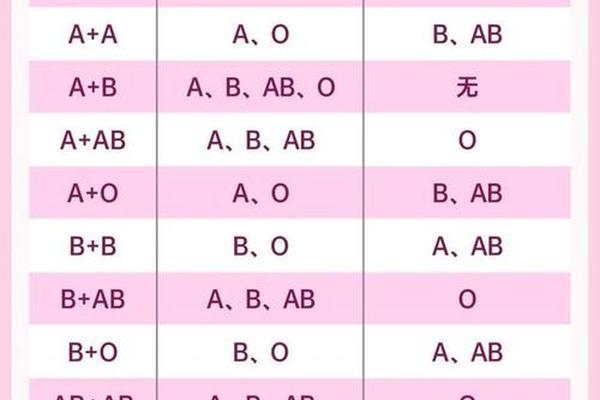
人类ABO血型系统自1900年被发现以来,始终是临床输血的基石。A型血与O型血的关系尤为特殊:A型红细胞表面携带A抗原,血浆中含有抗B抗体;O型红细胞缺乏A、B抗原,但血浆中同时存在抗A和抗B抗体。这种抗原-抗体的互补特性,决定了传统输血必须遵循“同型输注”原则,否则可能引发致命的溶血反应。

在极端紧急情况下,O型血曾被视为“万能血”。其原理在于O型红细胞缺乏A、B抗原,理论上不会与受血者血浆中的抗体发生凝集反应。这种认知存在严重误区。O型血浆中的抗A抗体若进入A型血患者体内,会攻击患者自身的红细胞,导致血红蛋白尿、肾功能衰竭等并发症。研究表明,输入200毫升O型全血即可使A型患者血浆中抗A效价显著升高,溶血风险增加5倍。现代临床仅允许在严格条件下输注O型洗涤红细胞,且总量需控制在患者血容量的10%以内。
二、酶工程技术突破血型壁垒
为解决O型血依赖性问题,科学家将目光投向酶工程技术。2019年,加拿大团队从肠道细菌Flavonifractor plautii中分离出两种酶,可在30分钟内清除A型红细胞表面90%的A抗原,将其转化为类O型血。这一突破的核心在于:肠道黏蛋白的糖链结构与红细胞抗原相似,细菌为获取营养进化出高效分解糖蛋白的酶系。
2024年丹麦团队的研究进一步优化了酶体系。他们发现的嗜黏蛋白阿克曼菌酶能同时处理A、B抗原及其“加长版”变异体,对B型血的转化效率达98%,A型血转化后免疫反应强度降低至传统方法的1/3。通过冷冻电镜解析,这些酶的活性位点具有独特的糖苷键识别域,使其切割精度比咖啡豆来源的酶提高20倍。转化血仍面临残留抗原检测难题,目前仅能通过质谱法确认抗原清除率,尚未达到临床普及标准。
三、临床实践中的风险控制策略
在现有技术条件下,A型血患者的输血管理需遵循分级预案。一级预案优先使用自体输血或A型同型血;二级预案启用O型洗涤红细胞,但需同步监测血浆游离血红蛋白和肾功能指标;三级预案仅在战地医疗等特殊场景考虑酶转化血。统计显示,采用分级策略的医院输血不良反应发生率可从0.12%降至0.03%。
交叉配血技术的进步为安全输血提供保障。微柱凝胶卡式法能检测低至0.1%的残留抗原,配合流式细胞术可实时监控输入红细胞存活率。对于需要多次输血的增生异常综合征患者,建议建立个性化抗原谱档案,通过基因组测序预判抗体产生风险。典型案例显示,某A型血老年患者接受累计5000毫升O型洗涤红细胞输注后,通过定期血浆置换仍保持血红蛋白稳定。
四、未来发展方向与挑战
血型转化技术正在向多维度突破。美国红十字会已启动“通用红细胞”计划,通过CRISPR基因编辑敲除ABO基因,但存在脱靶效应导致H抗原丢失的风险。我国科学家则尝试将纳米磁珠与酶耦合,开发出血型转化-抗原清除一体化设备,单次处理量可达200单位。
层面,转化血的身份认定引发争议。国际输血协会建议将酶处理血标注为“O-酶改型”,与天然O型血区分管理。经济学模型显示,当转化成本降至每单位100美元时,该技术可在全球挽救每年约17万例因血型不匹配导致的死亡。但这也可能削弱无偿献血体系,需通过政策引导平衡技术创新与传统献血的关系。
总结
从生物学机制到技术革新,A型血救治体系正经历深刻变革。O型血的“有限通用性”警示我们,任何医疗突破都需以精准风险控制为前提。酶工程与基因编辑的结合,预示着血型壁垒终将被打破,但这一过程中必须坚守“安全优先”的医学。未来研究应聚焦转化效率提升、残留抗原标准化检测、以及技术普惠性拓展,让更多患者受益于这场静默的血型革命。