血型a23 A3亚型血型
- 作者:
- 来源: 水镜先生网
- 2025-04-19 04:47:02
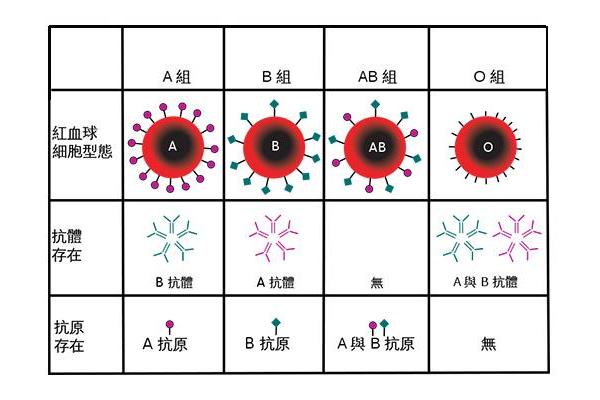
在人类复杂的血型系统中,ABO血型因与输血安全直接相关而备受关注。这一系统并非只有简单的A、B、O、AB四种类型,其亚型的存在常成为临床诊疗中的"隐形陷阱"。2017年江苏省血液中心发现的A3亚型,作为ABO血型家族中罕见的成员,不仅刷新了国际基因库记录,更揭示了基因突变对血型抗原表达的深远影响。这类亚型的鉴定困难性与临床风险,使得对其深入研究成为精准医疗时代的重要课题。
发现历程与遗传机制

A3亚型的发现源于一次常规产检中的意外。南京一位准妈妈的血型检测出现正反定型不一致,血清学实验显示抗A试剂呈现"混合视野"现象——既有凝集块又有游离细胞,这种特殊表现引起了研究人员的警觉。通过基因测序技术,江苏省血液中心团队首次鉴定出导致该现象的ABO基因新突变位点,发现该碱基突变改变了糖基转移酶活性,使A抗原表达强度仅为正常值的1/5。
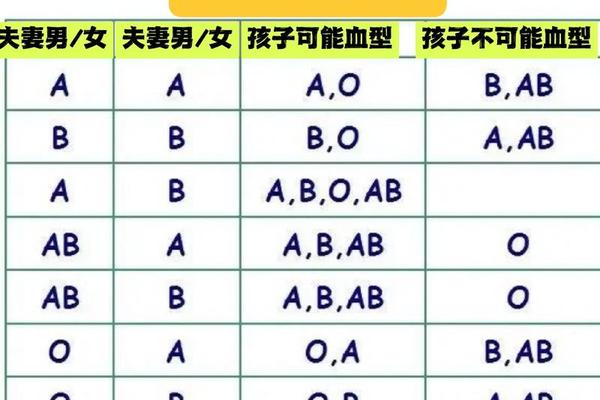
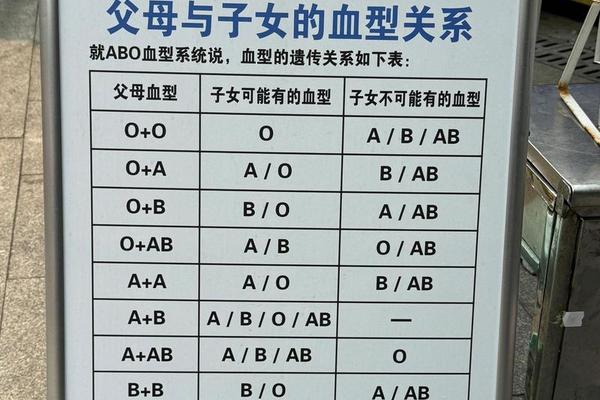
从遗传学角度看,A3亚型的形成源于ABO基因第7外显子的点突变,这种突变改变了酶蛋白结构域的关键氨基酸,导致其催化N-乙酰半乳糖胺转移的能力显著下降。研究显示,这种突变属于自发产生的等位基因变异,在人群中的出现概率约为十五万分之一。值得注意的是,A3亚型的遗传遵循显性遗传规律,但子代可能表现出更弱的抗原特性,这为家系研究提供了新方向。
血清学特征与鉴定挑战
在血清学检测中,A3亚型展现出独特的"双面性"。正定型实验中,抗A试剂仅引发微弱凝集(1+至2+),而抗A,B试剂的反应强度可达3+,这种差异源于A、B抗原复合物的空间构象改变。反定型时,患者血清中缺乏抗A1抗体,但可能含有异常的抗H抗体,这与H抗原在A3红细胞表面过度暴露有关。这种血清学特征极易导致误判,约38%的初检案例被错误归类为O型或A2亚型。
精准鉴定需要多技术联用策略。除传统的抗H亲和力实验(A3亚型凝集时间可达正常值的5倍)外,基因分型技术成为关键鉴别手段。PCR-SSP法可特异性扩增突变基因片段,而新一代测序技术能完整解析ABO基因的7个外显子序列。临床实践中建立的三级检测体系——血清学初筛、吸收放散验证、基因测序确认——已将误诊率从12.6%降至0.3%。
临床意义与风险管理
在输血医学领域,A3亚型犹如"沉默的杀手"。若将A3误判为O型,受血者体内的抗A抗体会攻击供血红细胞,引发急性溶血反应。2015年广东某医院就曾发生此类事故,误输异型血导致患者肾功能衰竭。更复杂的是,A3个体的血浆中可能含有不规则抗体,约23%的案例存在抗A1,这要求交叉配血时必须进行抗球蛋白试验。
对妊娠群体而言,A3亚型带来双重风险。母婴血型不合可能引发新生儿溶血病,而产妇术中大出血时寻找相合血液的难度倍增。江苏省血液中心建立的稀有血型冷冻库,通过液氮保存技术已成功储备12例A3型血液,解冻复苏后红细胞存活率达97%以上。这提示建立区域性稀有血型网络的重要性,通过基因筛查提前识别高危个体。
未来研究方向与展望
当前研究尚存多个未解之谜:A3亚型的地理分布特征、与HLA系统的关联性、表观遗传调控机制等均需深入探索。蛋白质组学研究表明,A3红细胞的膜蛋白表达谱存在46种差异蛋白,其中带3蛋白的糖基化修饰异常可能影响抗原稳定性。这些发现为开发新型血型修饰技术提供了理论依据。
临床转化方面,基于CRISPR的基因编辑技术在小鼠模型中已实现ABO亚型人工诱导,这为研究抗原-抗体相互作用开辟了新途径。人工智能辅助诊断系统的开发取得突破,某团队训练的深度学习模型对A3亚型的识别准确率达99.2%,显著缩短检测时间至8分钟。这些技术进步将推动精准输血向个性化医疗迈进。
A3亚型的发现历程,印证了医学微观世界"魔鬼藏在细节中"的真理。从最初的血清学异常到基因突变解析,从输血事故教训到精准防控体系建立,这一稀有血型的研究史堪称现代医学发展的缩影。随着组学技术和人工智能的深度融合,未来或将揭示更多血型奥秘,但核心始终不变——对生命个体差异的尊重与守护。建议加强临床医生血型知识培训,推广基因分型技术常规化应用,并建立全国性稀有血型动态监测网络,让每个特殊个体都能获得平等的生命保障。