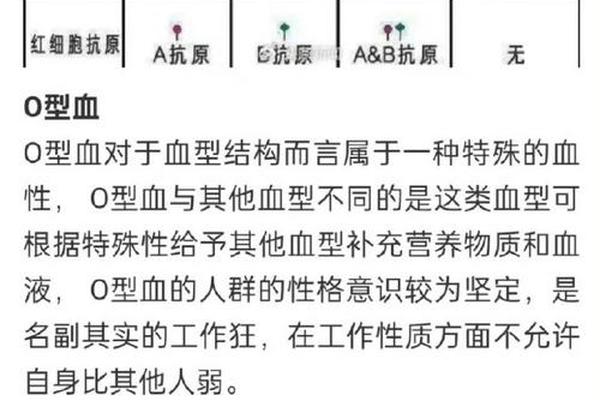
血型a抗原 ABO血型系统中的抗原和抗体
- 作者:
- 来源: 水镜先生网
- 2025-04-22 10:59:02
人类红细胞表面覆盖着复杂的糖链分子,这些分子构成了ABO血型系统的核心抗原。其中,A抗原的形成依赖于特定糖基转移酶的催化作用,其分子结构差异决定了不同血型个体间的免疫识别机制。作为免疫系统的"分子身份证",这些抗原不仅影响着输血和器官移植的成败,更与疾病易感性、进化选择等生命现象密切相关。自1901年兰德斯泰纳发现ABO血型以来,这个系统始终是免疫血液学研究的核心课题。
抗原结构的分子密码
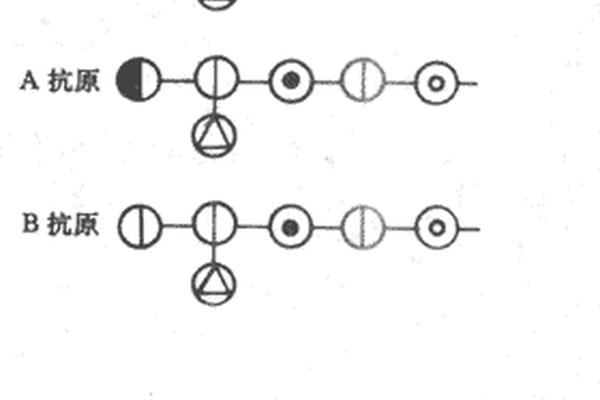
A抗原的分子本质是红细胞膜上糖鞘脂末端的三糖结构。在H抗原的岩藻糖基基础上,A型个体通过N-乙酰半乳糖胺转移酶的催化作用添加特定糖基,形成独特的抗原表位。这种精细的糖基化过程具有严格的遗传控制,ABO基因第7外显子的单核苷酸多态性(SNP)直接决定酶活性是否存在。
X射线晶体学研究显示,A抗原的三维结构具有特殊的空间构象。其末端N-乙酰半乳糖胺基团形成的β-1,3糖苷键,与B抗原的β-1,4半乳糖基形成镜像对称结构。这种微观差异在免疫识别中具有宏观效应:A型血清中天然存在的抗B抗体能够精确识别0.3纳米级别的结构差异,这种分子识别的精确性堪比抗体工程的定点突变技术。
免疫应答的双向机制
ABO血型系统的独特之处在于其天然抗体的存在机制。新生儿在6个月后逐渐产生针对非己抗原的IgM抗体,这种抗体产生不依赖抗原刺激,而是通过肠道菌群中类似抗原的交叉反应形成。2019年《Nature Immunology》的研究揭示,共生菌拟杆菌属的荚膜多糖与B抗原存在分子模拟现象,这解释了为何A型个体能自发产生抗B抗体。
在输血反应中,这种天然抗体引发急性溶血反应的效率令人震惊。1毫升不相容血液即可激活补体级联反应,导致每小时10亿红细胞的裂解速度。但有趣的是,器官移植时的超急性排斥反应却相对少见,这与血管内皮细胞抗原表达的可变性有关。东京大学团队发现,供体器官的缺血再灌注过程会下调ABO抗原表达,这种适应性改变为跨血型移植提供了理论依据。
临床医学的生死红线
血型鉴定误差导致的医疗事故始终是临床安全的重大威胁。美国血库协会统计显示,约1/15000的输血会出现ABO不相容,其中30%导致死亡。现代分子检测技术通过PCR-SSP法分析ABO基因型,将误判率降至千万分之一。但2018年哈佛医学院报告指出,嵌合体个体的存在仍可能造成假阴性结果,这提示表型与基因型检测必须联合应用。
在疾病关联性方面,A型血个体展现独特的流行病学特征。日本国立癌症研究中心追踪20万人群发现,A型个体胃癌发病率较其他血型高20%,这可能与幽门螺杆菌Leb抗原与A抗原的分子相似性有关。但2017年《柳叶刀》的孟德尔随机化研究提醒,这种关联可能存在混杂因素,需要更多全基因组数据支持。
遗传进化的选择印记
ABO基因座呈现典型的共显性遗传特征,但O等位基因在多数人群中占据优势。分子人类学研究揭示,ABO多态性形成于灵长类进化早期,其多样性可能与病原选择压力相关。2015年《Science》发表的尼安德特人DNA分析显示,远古人类已存在现代ABO多态性,提示该系统的进化优势超过30万年。
全球血型分布图呈现明显的地理梯度。欧洲的A型血高频区与腺鼠疫历史疫区高度重合,斯坦福大学团队通过体外实验证实,鼠疫杆菌Yersinia对A型红细胞的黏附率低60%,这可能是自然选择的重要证据。但非洲A型血高频区的形成机制仍有争议,疟疾选择假说与营养适应假说的论战仍在持续。
未来研究的突破方向
合成生物学为ABO血型研究开辟了新路径。2021年,加拿大科学家成功将猪红细胞改造成通用O型血,通过CRISPR技术敲除GGTA1和CMAH基因并保留H转移酶活性。这种人造血液在恒河猴实验中展现良好耐受性,但长期免疫安全性仍需验证。单细胞测序技术的进步,使得我们能够解析ABO抗原表达的时空差异,这为个体化输血提供了理论支撑。
在基础研究层面,ABO糖基化过程与癌症转移的关系备受关注。上海交通大学团队发现,A抗原能增强肿瘤细胞与血管内皮细胞的黏附,这种机制可能解释A型血患者某些癌症预后较差的现象。而针对ABO糖基化酶的抑制剂开发,正在成为抗癌药物研究的新热点。
ABO血型系统的研究史,本质上是人类解码生命密码的微观史诗。从输血安全的临床实践到人类进化的宏观图景,这个简单的抗原系统持续刷新着我们对免疫识别、疾病机制和自然选择的理解。未来研究需要整合结构生物学、群体遗传学和临床医学的多维视角,在精准医疗时代重新诠释这个百年经典课题的现代价值。正如诺贝尔奖得主巴鲁克·布隆伯格所言:"ABO系统是造物主留给人类的第一个生物识别码,我们至今仍在破译其中的生命智慧。