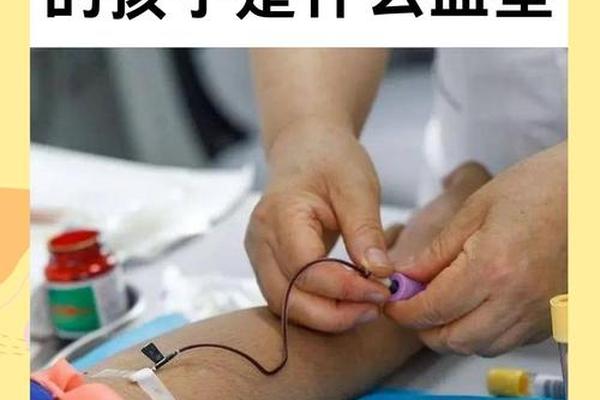
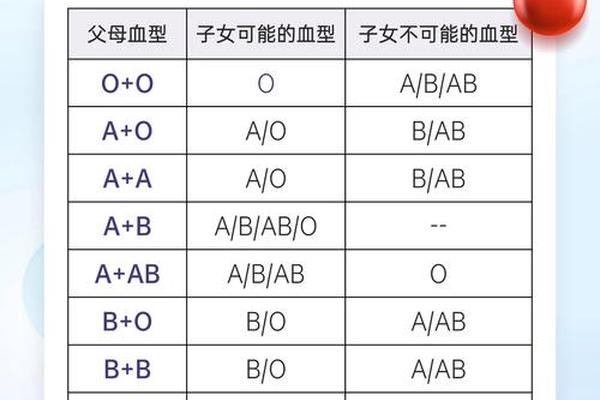
a血型的基因排列,A型血基因型IAi和IAA
- 作者:
- 来源: 水镜先生网
- 2025-04-26 18:30:01
ABO血型系统是人类最复杂的遗传多态性系统之一,其核心由IA、IB和i三个复等位基因构成。在A型血的基因型中,IAIA和IAi分别代表纯合显性与杂合显性两种遗传模式,这两种基因组合不仅决定了红细胞表面A抗原的表达强度,还与亚型分化、疾病易感性等生物学特征密切相关。理解IAIA与IAi的遗传规律及表型差异,对临床输血医学、法医学鉴定及疾病预防具有重要意义。
遗传机制与显隐关系
IA基因作为显性等位基因,其编码的α-1,3-N-乙酰半乳糖胺转移酶负责将A抗原前体转化为成熟A抗原。当个体携带IAIA纯合基因时,每个红细胞表面可形成81-117万个A抗原,而IAi杂合型的抗原数量约为纯合型的1/3。这种剂量效应源于基因拷贝数的差异:IAIA个体具有双倍剂量的A转移酶活性,而IAi个体仅有一个功能性等位基因。
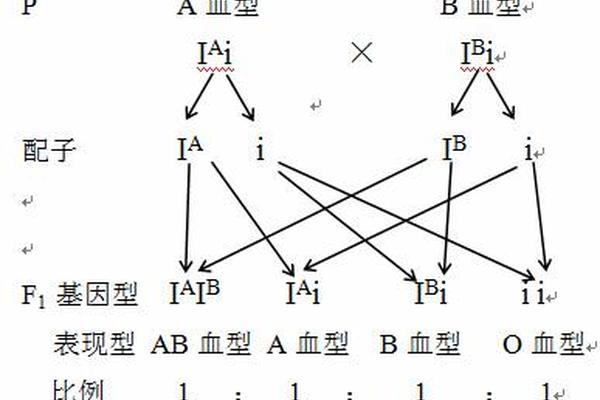
从孟德尔遗传规律分析,父母均为A型血时,若双方基因型均为IAi,其后代出现O型血(ii)的概率为25%。而若一方为IAIA,则所有子女必然携带至少一个IA基因,表现为A型或AB型血。这种遗传特性在亲子鉴定中具有重要价值,例如当父母均为A型却生育O型子女时,可直接排除IAIA基因型的存在。
亚型分化的分子基础
IA基因的突变与重组造就了复杂的A亚型系统。研究发现,IAIA基因型多对应于A1亚型,其红细胞同时表达A抗原和A1抗原,与双花扁豆凝集素产生强反应;而IAi基因型更易形成A2亚型,仅表达基础A抗原且抗原密度降低24%-65%。这种差异源于IA基因启动子区的甲基化修饰差异:IAIA的纯合状态可维持更高的表观遗传稳定性,而IAi杂合型易受调控元件变异影响。
在罕见的A亚型中,基因型与表型的对应关系更为复杂。例如Ax亚型虽携带IA基因,但因外显子剪切异常导致酶活性丧失99%,红细胞仅能通过吸收放散实验检测到微量A抗原。这类病例提示,单纯依靠基因型预测表型可能存在局限性,需结合血清学检测与分子诊断技术。
临床医学的双刃剑效应
IAIA与IAi的差异显著影响输血安全。A1亚型(IAIA)红细胞因抗原密度高,与A2个体血清中的抗A1抗体易发生急性溶血反应。统计显示,约2%的A2型个体会自然产生抗A1抗体,在紧急输血场景中,误将A1型血液输注给A2型患者可能引发致命后果。这要求血库必须采用单克隆抗A1试剂进行亚型鉴定。
近年研究还发现,IA基因与疾病易感性存在关联。全基因组关联分析显示,IA等位基因携带者早发性中风风险增加16%,可能与A抗原促进血小板活化及血管内皮黏附有关。但值得关注的是,这种风险在IAIA纯合个体中更为显著,提示基因剂量在病理机制中的放大效应。
基因编辑的突破前景
2025年东南大学吴国球团队取得突破性进展,通过工程化改造Flavonifractor plautii来源的N-乙酰半乳糖胺脱乙酰酶与半乳糖胺酶,可在5分钟内将A1型红细胞(IAIA)转化为通用O型。该技术的关键在于精确去除A抗原的N-乙酰半乳糖胺基团,同时保留H抗原结构完整性。冷冻电镜解析显示,融合酶的空间构象优化使催化效率提升28倍,为建立"人造O型血库"奠定基础。
未来研究需着重解决两个方向:其一是开发基于CRISPR-Cas9的基因编辑技术,直接修饰造血干细胞的ABO基因座;其二是建立多组学预测模型,通过整合H抗原分泌状态、Lewis血型系统等信息,精准评估IA基因型个体的输血风险与疾病易感性。
IAIA与IAi基因型的深入研究,揭示了ABO血型系统在分子遗传学层面的精妙复杂性。从抗原表达的剂量效应到亚型分化的表观调控,从输血安全的预警机制到基因编辑的技术革新,这些发现不断拓展着人类对血型生物学的认知边界。随着单细胞测序与合成生物学技术的进步,未来或将实现个体化血型改造与精准输血医学的深度融合,而IA基因的多效性研究也将为心脑血管疾病的早期干预开辟新路径。在此过程中,跨学科协作与框架的同步构建,将成为保障血型遗传学研究健康发展的关键支柱。