血型a为什么是ao a+血型是AA还是AO
- 作者:
- 来源: 水镜先生网
- 2025-04-28 13:34:02
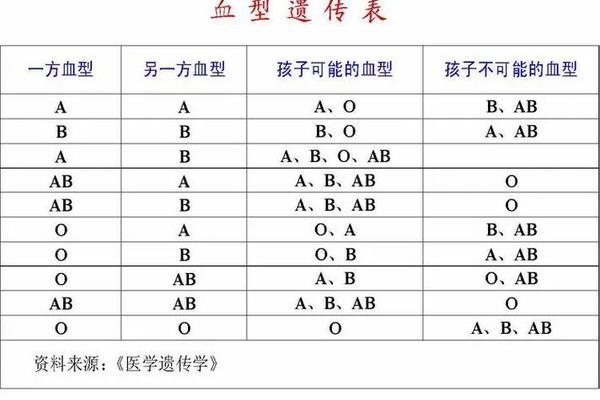
人类ABO血型系统的奥秘源于基因的显性表达与隐性传递。在遗传学中,A型血个体的基因型既可能是纯合显性(AA),也可能是杂合型(AO),而血型报告单上标注的"A+"则需拆解为ABO系统的"A"与Rh系统的"+"双重属性。这种看似简单的字母组合背后,蕴含着复杂的基因互作机制与抗原表达规律。理解这一遗传密码不仅能解释血型传递的生物学本质,更能为临床输血、器官移植及遗传疾病研究提供理论基础。
基因座位的双螺旋架构

ABO血型的遗传基础建立在人类第9号染色体长臂(9q34)的特定基因座上。此处存在三个等位基因:IA、IB和i,其中IA与IB为共显性关系,而i为隐性基因。根据孟德尔遗传定律,每个个体从父母各继承一个等位基因,形成六种可能的基因型组合。
当基因型为IAIA或IAi时,红细胞表面会表达A抗原,表现为A型血。前者属于纯合显性,后者则是杂合显性。这种显性表达机制源于IA基因编码的N-乙酰半乳糖胺转移酶活性,该酶能将H抗原转化为A抗原。值得注意的是,隐性基因i并不产生功能性酶,因此当个体携带IAi基因型时,显性基因IA的表达完全掩盖了隐性基因的作用。
显隐关系的分子生物学诠释
血型表达的显隐关系在分子层面呈现精密的调控机制。IA基因编码的转移酶能催化H抗原末端添加N-乙酰半乳糖胺,形成A抗原;而隐性i基因由于第258位碱基缺失导致移码突变,产生无功能的截短蛋白。这种酶活性的差异解释了为何杂合型IAi个体仍能完整表达A抗原。
Rh系统的阳性(+)特征则由独立遗传的RhD抗原决定。当个体携带至少一个RhD等位基因时(基因型为DD或Dd),即表现为Rh阳性。因此"A+"血型实为ABO系统与Rh系统的双重标识:A代表IA基因的表达,+代表RhD抗原的存在。两个系统的遗传互不干扰,这解释了为何同为A型血个体,Rh因子可能呈现阳性或阴性。
基因检测技术的突破性进展
传统血清学检测通过抗原-抗体反应判断血型,但无法区分纯合型(AA)与杂合型(AO)。现代基因检测技术如PCR-SSP(序列特异性引物扩增)和Sanger测序,可通过分析基因序列精准判定基因型。例如,通过检测第6外显子是否存在单核苷酸多态性(SNP),能明确区分IA与i等位基因。
2010年深圳血液中心研发的ABO基因检测试剂盒,采用多重PCR技术同时检测7个关键位点,其准确率达99.99%。此类技术对稀有血型鉴定尤为重要,如孟买型(hh)个体虽表型为O型,但基因检测可揭示其潜在的IA或IB等位基因携带状态。这解释了为何某些"O型"父母可能诞下A/B型子女。
临床实践中的特殊案例分析
在输血医学中,基因型差异可能引发隐性风险。例如,杂合型AO个体若输入纯合型AA供体的血液,虽ABO血型相符,但若涉及其他血型系统(如Kell、Duffy)的不匹配,仍可能引发迟发性溶血反应。器官移植时供受体间的基因型匹配度直接影响移植物存活率,纯合型供体更易引发免疫排斥。
亲子鉴定领域曾出现经典案例:B型父亲与"O型"母亲诞下A型婴儿,基因检测揭示母亲实为孟买型(hh基因型携带IA等位基因),父亲则为B型杂合(IBi),最终通过DNA分析确认亲子关系。这凸显了基因检测在破解表型-基因型矛盾中的关键作用。
未来研究方向与临床启示
当前研究正朝着两个方向深入:其一是探索血型基因与疾病易感性的关联,如A型血人群被证实具有更高的胃癌发病风险;其二是开发通用型人工血液,通过基因编辑技术敲除红细胞表面的ABO及Rh抗原。CRISPR-Cas9技术已在动物实验中成功制备"O型"通用红细胞,这或将成为输血医学的革命性突破。
对临床工作者而言,建议在以下场景实施基因检测:稀有血型确认、多次输血患者的精细配型、造血干细胞移植供体筛选等。普通人群则可通过基因检测了解自身血型的杂合状态,这对遗传咨询和家族健康管理具有重要价值。未来,整合多组学数据的血型预测模型,或将实现仅凭基因组数据即可推断全部36个已知血型系统的抗原表达谱。
血型作为刻写在基因中的生命密码,其解读已从简单的抗原分类发展为系统性的基因组学研究。理解A型血的AO/AA本质,不仅关乎遗传规律的认知突破,更将推动精准医疗时代的临床实践革新。在基因编辑技术与人工智能的双重驱动下,人类对血型奥秘的探索正迈向前所未有的深度与广度。