A血型的输血原则,血型亚型输血原则
- 作者:
- 来源: 水镜先生网
- 2025-05-01 02:32:02
血液作为生命活动的重要载体,其输注必须遵循严格的免疫学规律。在ABO血型系统中,A型血的抗原特性使其输血原则既遵循系统共性,又存在特异性要求。随着医学发展,血型亚型的发现进一步揭示了输血安全的复杂性。据统计,全球约32%的人口为A型血,而其中A2亚型占比约20%,这种生物学差异要求临床输血必须突破传统认知框架,构建更精细化的管理策略。
A型血的基本输血原则
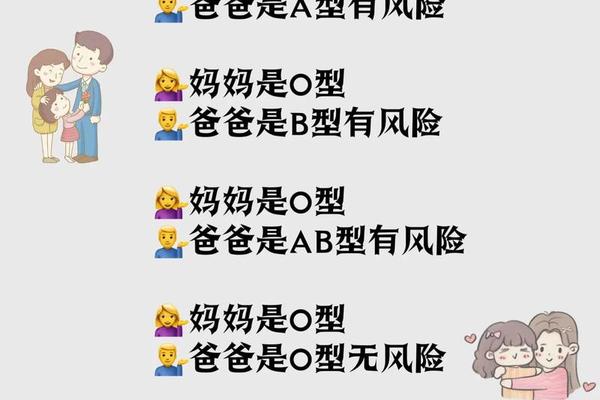
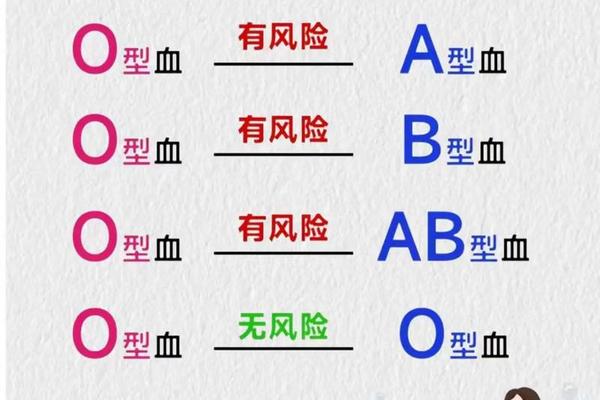
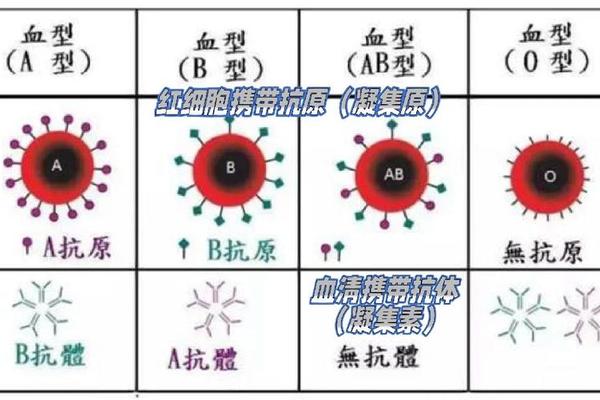
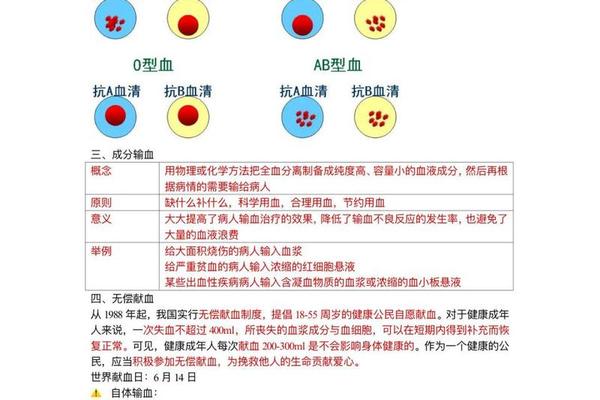
根据ABO血型系统的基本规律,A型血个体的红细胞表面携带A抗原,血浆中含有抗B抗体。这决定了其输血选择的核心逻辑:优先接受同型血液以避免抗原-抗体反应,紧急情况下可少量接受O型洗涤红细胞。值得注意的是,O型全血并非绝对安全,因其血浆中同时存在抗A、抗B抗体,可能引发溶血反应。
现代输血实践中,A型血的相容性需考虑双重维度。在红细胞输注方面,除严格同型外,O型洗涤红细胞因去除了血浆抗体而成为紧急替代方案;在血浆输注时,A型血浆可安全用于A型和AB型患者,但禁止用于O型或B型患者。这种双向选择机制体现了ABO系统的精妙平衡。
亚型差异对输血的深刻影响
A型血中存在A1和A2两大亚型,其抗原表达强度差异可达百倍。A1亚型红细胞表面A抗原密度约为1.0×10^6个/细胞,而A2亚型仅约2.5×10^5个/细胞。这种生物学特性导致两个关键临床现象:约1-8%的A2个体血清中存在抗A1抗体,可能引发输血反应;当A2亚型被误判为O型时,输注常规A型血将造成严重溶血。
对于亚型输血管理,国际输血协会提出三级验证标准。初次血型鉴定后,需通过吸收放散试验检测弱抗原,再以分子生物学方法确认基因型。特别是A2B亚型,其血清中可能含有抗A1抗体,输血时必须选择A2B或O型洗涤红细胞。临床数据显示,约0.3%的输血反应源于亚型误判,这凸显了精细分型的必要性。
Rh血型系统的协同作用
在Rh血型系统中,A型Rh阴性个体面临双重挑战。这类人群仅占全球人口的0.3%,其输血需同时满足ABO和Rh系统的相容性。当输入Rh阳性血液时,约70%受体会产生抗D抗体,导致后续输血风险倍增。育龄女性及需反复输血者必须严格输注Rh阴性血液,即便在紧急情况下也应控制阳性血液输注量不超过400ml。
Rh系统的复杂性还体现在抗体产生的时相差异上。首次输注Rh阳性血液的溶血反应潜伏期可达2-4周,这种迟发性反应常被临床忽视。研究显示,约15%的迟发性输血反应与Rh系统相关,其中A型血患者占比38%,这可能与A抗原对免疫系统的协同刺激作用有关。
交叉配血的必要性
交叉配血试验是突破血型静态认知的关键技术。该试验通过主侧(供者红细胞+受者血清)和次侧(受者红细胞+供者血清)双重验证,可检测出99.6%的血型不兼容情况。即便是同型输血,仍有0.02%的概率因其他血型系统(如Kell、Duffy系统)的抗体导致溶血,这使得交叉配血成为不可替代的安全屏障。
近年来的技术创新为交叉配血带来新突破。微柱凝胶技术的应用使检测灵敏度提升至0.01μg/ml抗体水平,较传统试管法提高两个数量级。分子配型技术则能提前预测Kidd、MNS等系统的潜在风险,将输血不良反应发生率从0.1%降至0.03%。这些进步正在重塑临床输血的安全边界。
未来发展方向与挑战
基因编辑技术为血型转换带来革命性曙光。2022年剑桥大学团队利用肠道细菌的糖苷酶成功去除A抗原,使A型血转化为通用型O型血,转化效率达97%。这种酶处理的红细胞在动物实验中存活率与天然O型血无统计学差异,为建立"通用血库"提供了可能。
在临床实践层面,自体输血技术值得深入推广。对于A型血手术患者,术前贮存式自体输血可完全规避异体输血风险。数据显示,当自体血储备量达预估用血量的60%时,异体输血需求下降82%。这种个体化输血策略,结合人工智能的用血评估系统,将推动输血医学进入精准化时代。
通过多维度解析A型血的输血原则,我们不仅需要恪守现有的免疫学规律,更要主动拥抱技术创新。从亚型分型的分子诊断到通用血型的生物工程,从交叉配血的智能化到自体输血的个性化,这些突破正在重新定义输血安全的内涵。唯有将严谨的临床实践与前沿科技深度融合,才能真正实现"零风险输血"的终极目标。