血型a a-怎么分辨(A(+)是什么血型)
- 作者:
- 来源: 水镜先生网
- 2025-04-23 08:16:02
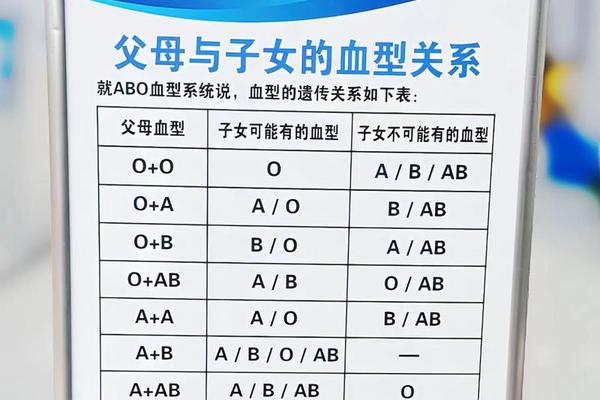
人类血型系统的复杂性源于红细胞表面抗原的多样性。目前国际公认的血型分类体系包含38种系统,其中ABO与Rh血型系统对临床医学影响最为深远。在ABO系统中,A型血的定义基于红细胞表面携带A抗原,血清中则存在抗B抗体;而Rh系统则通过红细胞是否携带D抗原来划分阳性和阴性。
A(+)血型的完整含义是ABO系统中的A型叠加Rh系统的阳性,即红细胞同时具备A抗原和RhD抗原。其对立概念A(-)则指ABO系统为A型但RhD抗原缺失的血型。这种双重分类体系的确立源于1900年兰德施泰纳对红细胞凝集现象的突破性发现,以及1940年Rh血型系统的补充完善。抗原的分子结构差异决定了血型的生物学特性,例如A抗原的核心结构是N-乙酰半乳糖胺,而RhD抗原则是镶嵌在红细胞膜上的跨膜蛋白。
二、血清学检测的技术路径
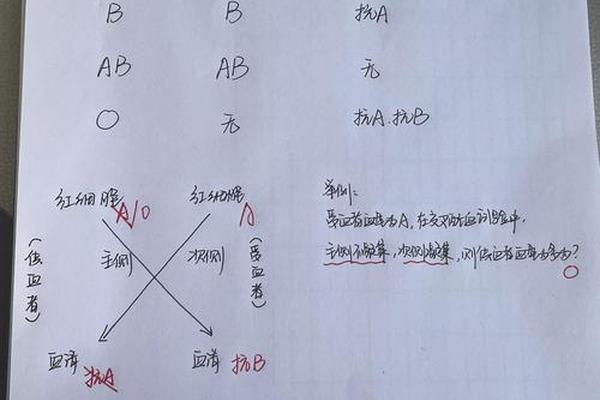
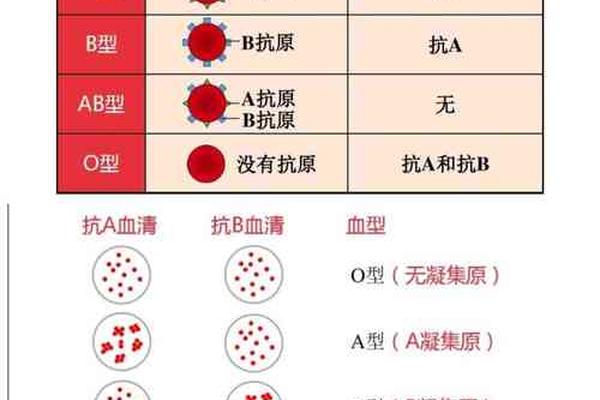
临床实践中,A型Rh阳性的判定需通过双重检测程序。首先采用单克隆抗A试剂进行正向定型,观察红细胞与试剂的凝集反应强度。典型A型血会呈现4+凝集,而某些亚型如A2型可能仅显示2+反应,此时需补充抗A1植物凝集素试验。RhD检测则使用IgM类抗D试剂,阳性结果表现为明显凝集,阴性则无反应。对于弱D或部分D变异型,还需进行间接抗人球蛋白试验确认。
特殊情况下需采用分子生物学检测。例如当血清学结果出现正反定型不符时(如抗A弱阳性而抗B阴性),需通过基因测序分析ABO基因外显子序列。2022年河南某医院发现的B(A)亚型案例显示,基因测序能准确识别640A/G位点突变,这种突变使B型转移酶获得合成A抗原的能力,导致血清学误判。此类技术突破使亚型检出率从传统方法的80%提升至99%以上。
三、Rh血型的遗传学规律
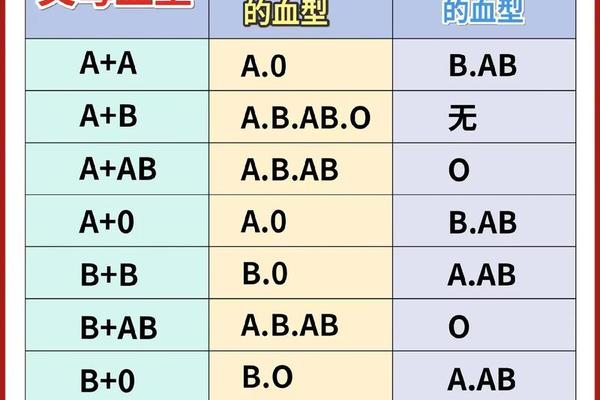
Rh血型的遗传遵循孟德尔显性遗传规律。Rh阳性由显性D基因决定,阴性则为隐性d基因纯合状态。当父母双方均为Dd杂合型时,子女有25%概率表现为Rh阴性。值得注意的是,Rh阴性在东亚人群中的发生率不足0.3%,显著低于白种人的15%。这种种群差异可能与历史上的自然选择压力相关,有研究指出Rh阴性个体对某些病原体的易感性更高。
血型遗传的复杂性在亲子鉴定中体现明显。若A型Rh阴性母亲诞下A型Rh阳性新生儿,需警惕父源RhD抗原引发的溶血反应。这种情况下,胎儿的RhD抗原可能通过胎盘进入母体,刺激产生IgG类抗D抗体,导致后续妊娠的新生儿溶血病。现代产前诊断已能通过母体外周血胎儿DNA检测提前预警此类风险。
四、临床输血的实践准则
在输血医学中,A(+)与A(-)的严格区分关乎生命安危。Rh阴性患者输入Rh阳性血液后,70%个体会在2-4周内产生抗D抗体,这种致敏化过程具有终身记忆性。育龄期女性Rh阴性患者必须严格输注Rh阴性血液,否则可能引发胎儿新生儿溶血病。统计显示,正确血型配型可使输血不良反应发生率从0.5%降至0.02%。
稀有血型库的建立成为现代血液管理的重点。我国建立的"熊猫血"数据库已收录超过10万Rh阴性献血者信息,通过冷冻保存技术可将红细胞保存期延长至10年。但A(-)型血液的临床供给仍面临挑战,某些地区库存满足率不足60%,这推动了人工血型改造技术的研究,例如使用酶法清除红细胞表面抗原。
五、血型研究的未来方向
血型抗原的生物学功能仍是未解之谜。最新研究表明,ABO血型可能影响新冠病毒受体ACE2的表达水平,O型个体感染风险较A型低20%。这种关联性提示血型抗原可能在病原体识别中发挥重要作用,其机制可能与糖基化修饰影响病毒刺突蛋白结合有关。
基因编辑技术为血型改造带来新可能。2023年日本团队成功将A型红细胞转化为O型,通过CRISPR技术敲除GTA基因编码的N-乙酰半乳糖胺转移酶。这种通用型血细胞的量产化,有望彻底解决稀有血型供给难题。但争议也随之产生,涉及基因改造血液的安全性和代际影响评估。
血型系统的精确认定是现代医学的基石。从血清学检测到基因分型,从遗传规律解析到临床输血实践,A(+)与A(-)的区分贯穿着生命科学的多个维度。随着单细胞测序和合成生物学的发展,未来或将实现个体化血型匹配和抗原定制化改造。建议加强稀有血型库的全国联网建设,同时推进血型相关的基础研究,特别是在感染免疫和肿瘤治疗领域的应用探索。对公众而言,了解自身血型不仅是健康管理的基本要求,更是对生命科学奇迹的认知见证。