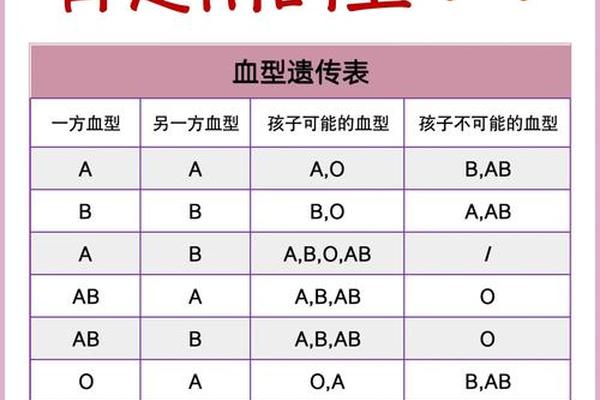
a型血无凝集b血型凝集;受血者为a型血,主侧不凝次侧凝集
- 作者:
- 来源: 水镜先生网
- 2025-04-23 17:53:02
血型鉴定与交叉配血的科学逻辑及临床意义
在医疗实践中,血型鉴定与交叉配血是输血安全的核心保障。当A型受血者的交叉配血试验出现"主侧不凝集、次侧凝集"的特殊现象时,这不仅揭示了ABO血型系统的复杂抗原-抗体反应机制,更对临床输血决策提出了精细化要求。本文将从基础原理、实验逻辑、临床风险及研究进展四个维度展开系统性分析。
一、ABO血型系统的抗原-抗体作用机制
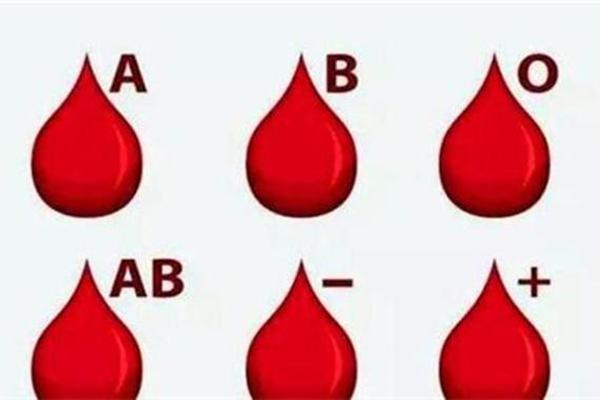
ABO血型系统的核心在于红细胞表面抗原与血浆抗体的特异性识别。A型血个体的红细胞表面表达A型凝集原(抗原),其血浆中天然存在抗B凝集素(抗体);B型血则呈现完全相反的抗原-抗体分布模式。这种抗原-抗体的对应关系源于基因编码的糖基转移酶活性差异:A型个体携带的N-乙酰半乳糖胺转移酶催化H抗原转化为A抗原,同时免疫系统对非自身抗原产生天然抗体。
当A型血液与B型标准血清接触时,抗A凝集素与A抗原的结合会引发红细胞凝集现象。这种反应具有高度的特异性,例如抗B抗体仅识别半乳糖结构的B抗原,而对其他糖基修饰无交叉反应。值得注意的是,O型血虽然缺乏A、B抗原,但其红细胞表面的H抗原前体可能在某些病理状态下引发弱凝集反应,这为交叉配血异常提供了潜在解释。
二、交叉配血试验的逻辑解析
交叉配血试验通过模拟输血过程中的双向免疫反应确保安全性。主侧试验(供血者红细胞+受血者血清)反映受血者抗体对供血者红细胞的攻击性,而次侧试验(受血者红细胞+供血者血清)则检测供血者抗体对受血者的潜在威胁。在A型受血者案例中,主侧不凝集表明供血者红细胞未携带A/B抗原(如O型血),次侧凝集则提示供血者血清含有抗A抗体(如O型或B型供血)。
这种现象的典型场景是O型供血者与A型受血者的配型。O型红细胞缺乏A/B抗原,故主侧无反应;但其血清中的抗A抗体与受血者A型红细胞结合导致次侧凝集。此时虽符合"少量缓慢输注"的紧急输血条件,但需警惕抗体效价过高引发的迟发性溶血反应。实验数据显示,约3%的O型献血者抗A效价超过1:256,这类血液输注给A型患者时次侧凝集强度可达+++以上。
三、临床输血的风险管控策略
主次侧配血结果的矛盾性要求临床采取分级应对方案。根据国际输血协会指南,当次侧凝集强度≤1+时,可在严密监测下限量输注200ml以内;若凝集强度≥2+则需更换供血者。我国《临床输血技术规范》特别强调,对于次侧弱凝集病例,必须进行抗体效价测定及抗球蛋白试验,排除自身抗体干扰。
风险管控的关键在于建立多维度评估体系。除常规盐水介质法外,采用聚凝胺法或抗人球蛋白法可提高不完全抗体的检出率。某三甲医院统计显示,应用增强检测技术后,次侧凝集的漏检率从12.3%降至1.8%。输血后需持续监测血红蛋白尿、发热等溶血征象,特别是在输注后2-24小时内的迟发性反应窗口期。
四、血型研究的前沿进展
近年研究发现,ABO血型抗原不仅存在于红细胞,还广泛分布于血管内皮、消化道上皮等组织,这为解释输血相关性微循环障碍提供了新视角。基因测序技术的进步使得H抗原缺失型(孟买型)等罕见血型的精准识别成为可能,相关检测成本已从万元级降至千元级。
在替代疗法领域,重组血型抗原酶的研究取得突破。2024年《自然·生物技术》报道的工程化糖基转移酶,可在体外将O型红细胞转化为通用型H抗原阴性细胞,动物实验显示其输血相容性提升40%。这为突破血型限制的"通用红细胞"制备奠定了技术基础。
血型系统的精密调控机制既是生命进化的杰作,也是临床治疗的挑战。从"A型血无凝集B血型凝集"的基础现象,到"主侧不凝次侧凝集"的复杂决策,每一步都彰显着免疫识别机制的精妙与临床风险控制的智慧。未来研究应着力于:①开发高灵敏度的床边快速抗体检测设备;②建立基于人工智能的输血风险预测模型;③推动合成生物学在血液替代品中的应用。唯有持续深化对血型系统的认知,才能在全球血液资源紧张的背景下,为患者构筑更安全的生命防线。